移植医療:日本と世界の現況
移植医療
・臓器移植:腎臓、肝臓、心臓の移植
ヒトや動物の健康な臓器を機能しなくなった臓器と交換し命を救おうとするもの
腎不全、肝不全、心不全
・組織移植:角膜移植、骨髄移植
・細胞移植:膵臓ランゲルハンス島細胞の移植、臍帯血移植、自己血液幹細胞移植、養子免疫療法
臓器移植、人工臓器と再生医療
血液透析 ー 人工腎臓:慢性腎不全に対して、血漿をフィルターでろ過してBUNなどを排除する。
人工心臓、人工肝臓、人工心肺 ー 一時的な使用
再生医療:組織再生、Tissue Engineering ‐ 幹細胞 + Scaffold + 成長因子Growth factorで必要な組織を培養して作る。骨、歯、肝?本人の細胞を使うことができる。
動物でヒトの臓器を作る?
胎生幹細胞Embryonal Stem Cellからあらゆる臓器を作り出すことが将来可能になるか?
臓器移植の歴史
1902年:オーストリアの外科医Ulmannがイヌの腎臓を摘出し、同じイヌの首に移植する実験を行った
1905年:フランス人(後に米国へ)のCarrelはイヌ、ネコで腎移植:一時正常に機能するがやがて何らかの生物学的因子で機能しなくなる→拒絶反応
1906年:フランス人Jaboulayはヒツジ、ブタからヒトへの異種間腎移植を試みる
1910年:京都大学の山内半作、第11回外科学会で臓器移植実験を報告
1936年:ウクライナのVoronoyは急性腎不全患者を救うため死者から摘出した腎臓を患者の大腿部に移植したが、36時間後に死亡
1940年代:イギリス(後に米国)Medawarによる移植免疫拒絶反応の解明
1954年:米国MerrillとMurray、一卵性双生児間の腎臓移植に成功
1956年:新潟大学の楠隆光、井上彦八郎による腎臓移植の臨床
1961年:英国CalneがアザチオプリンAzathioprineが実用的な免疫抑制剤であることをイヌの腎移植で証明
1963年:米国Murrayによってヒトの腎移植でアザチオプリンを使用
1963年:米国Starzlは胆道閉鎖症幼児で肝移植を行うが死亡。その後も彼は肝移植を続け1967年400日生存を記録。1970年代終わりまでにケンブリッジ大のCalneとともに肝移植の手技を確立
同年肺移植第1例
1964年:千葉大の中山恒明らによる心停止後の肝臓移植日本第1例 東京大学の木本誠二らによる慢性腎不全に対する腎移植日本第1例
同年膵移植第1例
1967年:米国Starzlが肝移植に初めて成功
南アフリカBarnardによる世界初の心移植。18日間生存
1968年:Barnardの2例目が9ヶ月生存。世界で約100例の心移植が行われるが、拒絶反応で死亡
同年日本で札幌医大の和田寿郎による日本初の心移植
同年ハーバード大学で脳死基準作成
1970年:スイスの製薬会社サンド・ファーマ社の社員が採取したノルウェーの土壌から生えた真菌(カビ)が、シクロスポリンAという物質をつくりだした
1972年:同社研究員BorelはCyclosporin Aが強力な免疫抑制作用を持つことを発見
1978年:Calneは死体腎移植でCyAを使用。1979年には死体肝移植でも使用
以後臓器移植の成績が飛躍的に向上する
1980年:Starzlは肝臓移植にシクロスポリンとステロイドを併用し、好成績を得た。スターツルの報告によると、肝臓移植の1年生存率がアザチオプリンの使用では38%だったのが、シクロスポリンで78%と、飛躍的に向上した
1980年:Shumwayが心臓移植に使用して、1年生存率が80%を超える成績を収めた
1983年ごろからシクロスポリンが薬剤として普及し、世界各地で使われるようになった
現在は日本の藤沢薬品が開発した免疫抑制剤FK506 (Prograf)がシクロスポリンよりも強力な薬として普及している
ドナーとレシピエント
・血液型の一致
・HLA(Human Leukocyte Antigen、MHC Major Histocompatibility Complex主要組織適合抗原とも呼ばれる)の一致
ただし、必ずしも100%一致していなくても可能なことが多いが、拒絶反応が起きやすい。
また、移植臓器中に含まれる免疫担当細胞がレシピエントの組織に対して免疫反応を引き起こし、移植片対宿主反応Graft-versus-host reaction (GVH)が起きて組織障害が起きることがある。
HLA class I & class II
HLA: human leukocyte antigen
MHC major histocompatibility complexとも呼ばれる。
Class Iはほとんどすべての体細胞に表現されている。A,B,C locus
Class IIはBリンパ球、マクロファージ、樹状細胞など一部の細胞に表現されている。DR,DQ,DP locus
個人個人で異なるほど多形性ががあり、同じ型を持つ人は約4-5万人に一人しかいない。一卵性双生児は同一。
HLAが異なると、移植片に対して拒絶反応が起きる。GVH(graft-versus-host)反応も同様。
日本における移植医療の必要性
腎移植
適応疾患:すべての末期腎不全
腎移植:日本では1996年現在、167,192人が人工透析(血液透析)を受けている。このうち14,429人が死体腎移植(献腎移植)を希望して献腎移植希望登録を行なっている。
日本では生体腎移植、死体腎移植あわせて年間700から1000例施行されている。
米国では年間10,000例、ヨーロッパでは年間12,000例施行。80-90%が死体腎移植。
肝移植
適応疾患:先天性胆道閉鎖症(年間発生数120)、先天性代謝異常症(数十)、原発性胆汁性肝硬変症(500)、原発性硬化性胆管炎(ごく少数)、劇症肝炎(1,500)、肝硬変症(年間死亡者4,500)
年間肝移植適応例の2,300人が移植を受けられないため死亡している
日本では年間120人が肝移植を受けている(外国施行例も含め)。近年、生体肝移植が多数を占めている。
米国、ヨーロッパでは年間それぞれ4,000人。
心移植
拡張型心筋症、虚血性心疾患、その他の疾患のため心臓機能が荒廃し従来の治療法では治せないか進行を抑えられない末期的状態にあり、以下のいずれかの条件を満たす場合心臓移植が適応となる。
(ア)長期間またはくり返し入院治療を必要とする心不全
(イ)β遮断薬およびACE阻害薬を含む従来の治療法ではNYHA (New York Heart Association) 3度ないし4度から改善しない心不全
(ウ)現存するいかなる治療法も無効な致死的重症不整脈を有する症例
年齢は60歳未満
ほかの臓器障害を合併していないこと、本人および家族の心臓移植に対する十分な理解と協力が得られること
心移植施行例数
日本での年間新規患者発生数は推測で205〜670人(1966年)
移植待機中の1年生存率は47%
米国では年間約23,00例の心移植が行われているが、待機中に約750名が死亡している。
米国における主な臓器移植症例数の推移
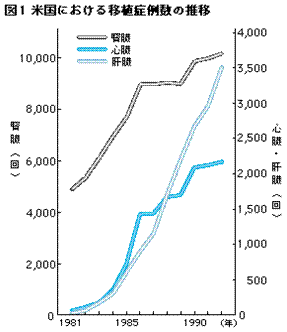
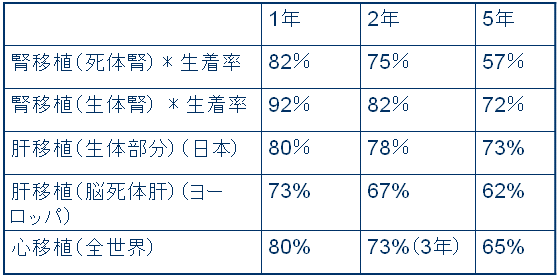
臓器移植の治療成績
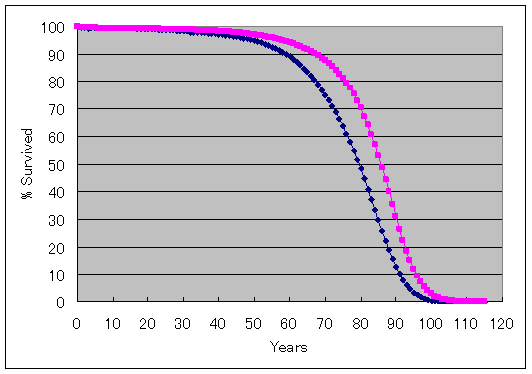
日本人の生存曲線
第18回日本人の生命表に基づく。
日本における法整備
日本では:法の整備が遅れた
1990年: 厚生省は「臨時脳死及び臓器移植調査会(脳死臨調)」を組織
1992年1月22日に「脳死を人の死とすることについて概ね社会的に受容され合意されている」として、一定の条件下における脳死体からの臓器移植を認める趣旨の答申が提出され,これを受けて答申を尊重し本問題に取り組む旨の方針が閣議決定された。
1992年12月:「脳死及び臓器移植に関する各党協議会(各党協議会)」が発足し「臓器移植法案(仮称)要項(案)」がとりまとめられた。
法の制定
1994年4月:「臓器の移植に関する法律案」が議員立法の形で第129回通常国会に提出されたが議決にいたらず、継続審議となった。
1995年6月:衆議員厚生委員会において提案理由の説明、同月13日には参考人からの意見聴取が行われた。
平成9年7月16日 法律第104 、「臓器移植に関する法律」 成立。
臓器移植に関する法律:25条から構成
臓器の摘出 第6条
1 医師は、死亡した者が生存中に臓器を移植術に使用されるために提供する意思を書面により表示している場合であって、その旨の告知を受けた遺族が当該臓器の摘出を拒まないとき又は遺族がないときは、この法律に基づき、移植術に使用されるための臓器を、死体(脳死した者の身体を含む。以下同じ。)から摘出することができる。
2 前項に規定する「脳死した者の身体」とは、その身体から移植術に使用されるための臓器が摘出されることとなる者であって脳幹を含む全脳の機能が不可逆的に停止するに至ったと判定されたものの身体をいう。
脳死
脳死とは
脳(中枢神経系)=大脳、小脳、中脳、橋、延髄、脊髄
脳幹=中脳、橋、延髄
脳幹:呼吸、循環などの生命に直結する機能の中枢。脳幹の機能が失われると呼吸が止まって生存不可能の状態になる
全脳死:大脳、小脳、脳幹を含む全脳髄の不可逆的な機能停止。(*全中枢神経死、脳幹死)
脳死と心臓死
「心臓死、すなわち心拍と呼吸の不可逆的停止は、患者の全体としての死を意味する」というのが従来の死の概念である
心拍と呼吸が停止しても直ちに体の全細胞が死んでいるわけではない
同様に、脳死を脳幹機能の不可逆的停止、大脳を含めた脳全体の機能停止は、脳の全細胞が直ちに死ぬことを意味するのではない。
脳のあらゆる細胞が死ぬことが脳死というわけではない
脳死になると
人工呼吸器(レスピレータ)を付けないと呼吸が停止し、数日で心臓も停止する。最長でも100日。
脳幹を含む全脳の血流が不可逆的に途絶し、脳が融解壊死に陥る。
なお、植物状態では大脳は機能停止しているが、呼吸をつかさどる脳幹は機能しているので、呼吸機能、あるいは循環系のコントロールは、正常、あるいは正常に近い状態で働いている。栄養を与えれば生存可能。
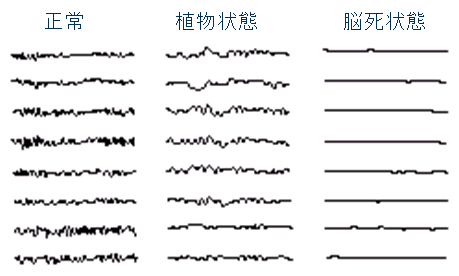
脳死の判定
脳死の判定ー前提条件と除外例
1.器質的に脳が障害されている
2.深昏睡・無呼吸である
3.脳障害の原因が確実に診断されている
4.適切な治療をもってしても回復不能である
除外例
1.6歳未満の小児
2.薬物中毒、32℃以下の低体温、代謝・内分泌障害などの症例
脳死判定基準
痛み刺激にも反応しない深昏睡
脳幹の機能を反映する自発呼吸が、完全に停止している
人工呼吸器をはずして、無呼吸テストを行う。動脈血の炭酸ガス分圧が60mmHg以上になっても自発呼吸の出現がなければ、自発呼吸がないと判断する
瞳孔が固定している
すべての脳幹の反応が消失している。角膜反射など7つの脳幹反射の検査を行う。(1) 対光反射の消失2) 角膜反射の消失3) 毛様脊髄反射の消失 4) 眼球頭反射の消失 5) 前庭反射の消失6) 咽頭反射の消失 7) 咳反射の消失)
脳波が平坦である
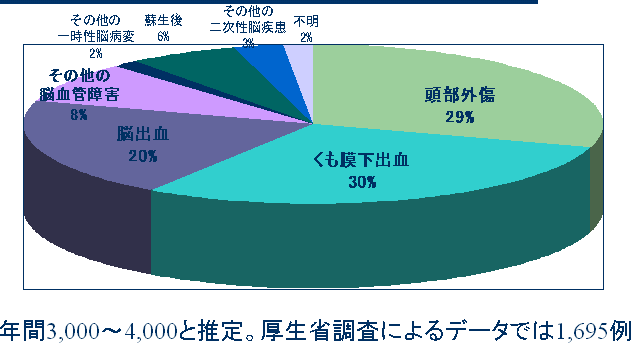
日本における脳死の原因疾患
脳幹反射
1)対光反射:瞳孔に光を当てると縮瞳する。
2)角膜反射:求心性神経は三叉神経で、遠心性神経は顔面神経である。綿球または綿捧の先端をよって細くしたものを眼球角膜部に触れると、瞬目する反射である。
3)毛様脊髄反射:頸部付近をつねるか針で疼痛刺激を加えると、両側の瞳孔散大が起こる。この反射が消失している場合には下部脳幹の障害を意味する。
4)眼球頭反射:求心性神経は主に前庭神経で、固有感覚受容性求心路(頸部)も関与している。遠心性神経は動眼神経、滑車神経、外転神経である。意識障害があり、外眼筋麻痺のない場合には、頭を受動的に急速に左右に回転すると、眼球は運動方向と逆方向に偏位する。
5)前庭反射:求心性神経は前庭神経で、遠心性神経は動眼神経、滑車神経、外転神経である.頭部を30度挙上し、カテーテルで外耳道に冷水を50ml以上注入する。意識障害があっても脳幹機能が保たれている場合には、眼球が刺激側に偏位する.脳死では眼球運動が全くみられない。
6)咽頭反射:吸引用カテーテルで咽頭後壁を刺激すると、咽頭筋が収縮し、吐き出すような運動が起こる。舌咽・迷走両神経およびその神経核の検査である。
7)咳反射:主に迷走神経が関与する反射である。気管内吸引用カテーテルで気管を刺激した場合に咳が起こる。聴性脳幹反射 ABR(auditory brainstem response)
ヘッドホンでカチカチとクリック音を聴かせると、脳幹が機能していればそれに反応して脳波が出てくる。
I波からVII波まであり、I波は聴神経の反応
II波以下は脳幹のいろいろな部位の活動の度合いに応じて機能が反映される。I波からV波までは、脳幹のどの部位で発生するかが分かっているが、VI、VII波の由来は定かではない。 脳死者の約70%では、I波からVII波まで全部が消える。残りの約30%は、I波を残してII波からVII波が消える。
脳死の診断基準に加えて、できるだけ本検査を取り入れることが望ましいとしている。ただし、必須ではない。 他にも、脳血管撮影、超音波ドプラ法などの脳血流を調べる検査法がある
脳死判定のプロトコール
1回目の脳死判定→医師2人が確認の署名
6時間以上間隔をおいて
2回目の脳死判定→医師2人が確認の署名
総合判定→1回目と2回目の結果を見て、2人の医師が「確かに脳死に間違いない」ことを総合判定して署名
延べ6名の医師の署名によって、脳死診断が確定される
臓器移植の普及
日本臓器移植ネットワーク
1995年4月に(社)日本腎臓移植ネットワーク
1997年10月16日に「臓器の移植に関する法律」が施行されて以降、全ての臓器を対象とする(社)日本臓器移植ネットワークに変わる
移植医療を公平で公正にそして円滑に推進するための、日本ではじめての第三者機関
日本臓器移植ネットワークの仕事
臓器移植についての普及・啓発
移植希望者の登録とそのデータベースの維持管理
コーディネーターの派遣
臓器摘出チームの編成・召集、臓器や検査用血液の搬送の手配
ドナーカード
脳死後臓器を提供する場合、本人が生前にそれを希望することを書面で残しており、しかも遺族がそれを承諾しなければならない。




